Бактериофаг MS2 – средство доставки для таргетной химиотерапии солидных опухолей
РЕФЕРАТ Бактериофаг MS2 был использован для таргетной доставки индуктора апоптоза, Tl+, в ткань опухоли. Таргетная доставка обеспечивалась iRGD-пептидом, лигандом интегринов, локализуемых преимущественно на поверхности эндотелиоцитов новообразованной сосудистой сети в опухолевой ткани и некоторых опухолевых клетках. Синтезированный пептид конъюгировали с капсидными белками MS2. Ионы Tl+ из TlNO3 проникали внутрь частиц фага и прочно связывались с его РНК. Препараты MS2, модифицированного пептидом и наполненного Tl+, вызывали гибель культивируемых клеток двух типов рака молочной железы человека и некроз ксенографтов этих опухолей. Ни конъюгат бактериофага MS2 с пептидом без Tl+, ни заполненный Tl+ фаг без пептида, ни он же с неконъюгированным пептидом в растворе не вызывали таких эффектов. Препарат не проявлял острой токсичности в терапевтической дозе
СПИСОК СОКРАЩЕНИЙ ED50 – эффективная доза (effective dose), при которой эффект составляет 50% от максимально возможного; LD50 – доза вещества, введение которой вызывает гибель 50% животных; SDS – sodium dodecyl sulphate (додецилсульфат натрия); БОЕ – бляшкообразующие единицы; ВЭЖХ – высокоэффективная жидкостная хроматография; ДМАИ – диметиладипимидат; РМЖ – рак молочной железы.
ВВЕДЕНИЕ В последние годы усилия разработчиков противоопухолевых лекарств сконцентрированы на препаратах направленного действия на основе как новых, так и уже известных цитостатиков [1]. Наиболее эффективным способом доставки считается использование наноконтейнеров, модифицированных специфичными лигандами (липосом, мицелл, полимерных наночастиц, вирусоподобных частиц, вирусов), заполняемых лекарственными соединениями [2]. Однако применение инновационных средств доставки не решает проблему множественной лекарственной устойчивости опухолей, способную свести на нет все усилия по повышению эффективности лекарственных соединений [3]. Показано, что ионы Tl+ обладают мощным цитотоксическим действием и подавляют функционирование белковых насосов лекарственной устойчивости опухолевых клеток [4]. Включение Tl+ в «не протекающий» наноразмерный контейнер, снабженный системой направленной доставки, позволит создать эффективное средство для разрушения опухолей при значительном снижении токсического воздействия Tl+ на организм в целом. В 1980-х гг. удалось наполнить Tl+ частицы вируса осповакцины [5]. Механизм наполнения заключался в образовании прочного соединения между Tl+ и вирусной РНК [6]. В качестве наноконтейнера нами был выбран бактериофаг MS2, способный размножаться только в клетках Escherichia coli, несущих F-пили и не являющихся симбионтами либо патогенами человека [7]. Направленность доставки обеспечивали конъюгацией капсидных белков фага с пептидом (Gly) 3 -iRGD, содержащим фрагмент cycloSS-(CRGDKGPDC) (iRGD), ответственный за связывание с интегринами, локализованными преимущественно на внешних мембранах эндотелиоцитов вновь формируемой патологической сосудистой сети солидных опухолей и на ряде опухолевых клеток [8]. В нашей работе проведена экспериментальная проверка эффективности наполненного Tl+ фага MS2 с адресным пептидом в качестве потенциального противоопухолевого препарата.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ Получение бактериофага MS2 описано в работе [9]. Количество бляшкообразующих единиц (БОЕ) в 1 мл препарата фага определяли методом титрования в агаровых слоях. Пептид (Gly)3-iRGD получали методом автоматического твердофазного синтеза исходя из 9-флуоренил(метоксикарбонил)-аминокислот (ChemPep, США) (синтезатор 433А, Applied Biosystems, метод FastMoc). Формирование S–Sмостика проводили путем окисления I2 [10]. Пептид очищали ВЭЖХ на обращенной фазе (колонка C18 Triart, 21 × 250 мм, 10.0 мкм, YMC, Швейцария, рабочая станция Agilent 1100, Agilent, США) в градиенте концентрации CH3 CN (BioSolve, Израиль) в воде в присутствии 0.1% уксусной кислоты. По данным аналитической ВЭЖХ на обращенной фазе (колонка C18 Triart, 2.1 × 50 мм, 2.0 мкм (YMC), рабочая станция Agilent 1200) с УФ- и масс-спектрометрической детекцией чистота препарата пептида не ниже 95%. Конъюгацию пептида (Gly)3 -iRGD с капсидными белками фага MS2 проводили с использованием гомобифункционального реагента диметиладипимидата (ДМАИ, Sigma, США) в молярном соотношении белок фага : пептид: ДМАИ 1 : 20 : 80 по методике [11]. Бактериофаг отделяли от избытка реагентов осаждением 25% раствором полиэтиленгликоля 6000 («Диа-М», Россия) с 1 М NaCl. Осажденный бактериофаг суспендировали в деионизованной воде. Заполнение бактериофага Tl+ проводили с использованием TlNO3 (Sigma-Aldrich, США). Бактериофаг MS2, конъюгированный с пептидом (iRGD-MS2), в количестве 1011 БОЕ инкубировали в 3 мл 0.5 мкМ раствора TlNO3 (5 ч при 38о С) с последующим осаждением, как указано выше, и диализом против фосфатно-солевого буфера (0.14 М NaCl, 0.01 M фосфат натрия, рН 7.4). Количество включенных в вирионы и присутствующих в среде Tl+ определяли согласно [12]. Суспензию наполненных Tl+ частиц фага центрифугировали в течение 10 мин при 5000 об/мин для удаления осадка солей таллия, разводили 50 мМ буфером трис-HCl, рН 9.0 до концентрации (условно) 108 БОЕ/мл, денатурировали нагреванием в течение 30 мин при +70о С с РНКазой в 0.05% SDS, затем регистрировали тушение флуоресценции (длины волн возбуждения – 340 нм, эмиссии – 465 нм, спектрофлуориметр UV-1900, Shimadzu, Япония) натриевой соли 1,3,6,8-пирентетрасульфоновой кислоты (BOC Sciences APP, США) ионами Tl+. По калибровочной кривой зависимости степени тушения флуоресценции 1,3,6,8-пирентетрасульфоновой кислоты от [Tl+] рассчитывали количество Tl+ в препарате фага. Количество Tl+ в буферном растворе после диализа определяли без предварительной денатурации. Цитотоксическое действие iRGD-MS2-Tl+ на клетках в культуре исследовали на линиях MCF-7 (гормонзависимый рак молочной железы (РМЖ)) и МDA-MB-231 (гормоннезависимый РМЖ). Клетки культивировали в бессывороточной среде (MSC1 Pan BioTech) и в той же среде с 5% фетальной сыворотки телят. Препарат iRGD-MS2-Tl+ вносили в 10-кратных разведениях, начиная с концентрации 108 БОЕ/мл. В качестве контроля использовали препарат iRGD-MS2 (фаг, конъюгированный с пептидом, без Tl+). Погибшие клетки подсчитывали после окрашивания Эвансом синим. Противоопухолевое действие препарата iRGDMS2-Tl+ тестировали на мышах nude c MCF-7- или МDA-MB-231-ксенографтами. Мышам внутрикожно вводили 105 –106 клеток MCF-7 или МDA-MB-231, а через 14 дней мышам опытных групп в течение 10 дней 1 раз в день вводили внутрибрюшинно по 200 мкл суспензии, содержавшей iRGD-MS2-Tl+ в количестве, соответствующем 108 БОЕ/кг, контрольным – iRGD-MS2, MS2-Tl+ или MS2-Tl+ + iRGD (в растворе, 2 мкг/кг) в таком же количестве и объеме раствора. В каждой опытной и контрольной группах было по 11 животных. Некротическую активность препарата определяли как отношение площади некротизированной ткани к общей площади опухоли через 12 дней после окончания введения препаратов фага по результатам анализа цифровых изображений гистологических срезов, сканированных на ScanScope CS2. Предварительное исследование острой токсичности препарата iRGD-MS2-Tl+ проводили на 10 крысах (самках) WKY (Wistar-Kyoto) весом 200– 250 г. Крыс содержали в условиях 12-часового светового дня на стандартном лабораторном корме и воде ad libitum. Однократно внутрикожно вводили 108 БОЕ/животное в объеме 500 мкл. Регистрировали состояние животных в течение 3 недель с момента введения препарата. Эксперименты на животных проводили в соответствии с Международными рекомендациями Европейской конвенции по защите позвоночных животных, используемых при экспериментальных исследованиях, и правилами надлежащей лабораторной практики (GLP) в РФ, утвержденных приказом Минздрава РФ № 267 от 19.06.2003.
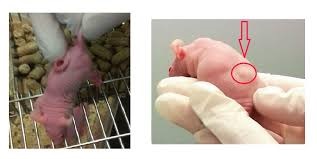
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ В результате инкубации бактериофага MS2 (как модифицированного, так и не модифицированного пептидом iRGD) в среде с TlNO3 получены препараты MS2, содержавшие Tl+ в количестве 2.0 × 10-9 г-экв таллия в расчете на 108 БОЕ. Количество Tl+ на 1 БОЕ составило 2.0 × 10-17 г-экв (≈4 фг на 1 БОЕ, т.е. 400 нг в 108 БОЕ). В буферном растворе, против которого диализовали наполненный таллием бактериофаг, Tl+ не обнаружен, что свидетельствует о его прочном связывании с РНК фага внутри частиц MS2. Как видно из рис. 1, в бессывороточной среде препарат iRGD-MS2-Tl+ проявлял цитотоксическое действие на клетки и гормонзависимого, и гормоннезависимого РМЖ. В случае гормонзависимого РМЖ (клетки MCF-7) ED50 препарата iRGD-MS2-Tl+ составляла чуть менее 105 БОЕ/мл культуральной жидкости, а статистически значимое превышение цитотоксического эффекта препарата по сравнению с контролем наблюдалось вплоть до концентрации 10 БОЕ/мл. Клетки гормоннезависимого РМЖ МDAMB-231 были более устойчивыми к действию препарата: ЕD50 для этих клеток в бессывороточной среде составляла 106 –107 БОЕ/мл, а статистически значимое превышение цитотоксического эффекта препарата над контролем наблюдалось до концентрации 104 БОЕ/мл. В среде с сывороткой цитотоксическое действие iRGD-MS2-Tl+ проявлялось намного слабее, что может свидетельствовать о конкуренции между компонентами сыворотки и частицами iRGD-MS2-Tl+ за проникновение в клетки. У мышей с ксенографтами MCF-7 и МDA-MB-231 через 12 дней после введения препарата iRGDMS2-Tl+ наблюдалось уменьшение объема опухоли по сравнению с контрольными группами животных (рис. 2). Гистохимически показано некротизирующее действие iRGD-MS2-Tl+ на соответствующие опухоли. Из рис. 3 видно, что препарат iRGD-MS2-Tl+ вызывал некроз ткани опухоли (р < 0.05) более эффективно, чем препараты фага с пептидом, но без Tl+, фага с Tl+, но без пептида, фага с Tl+ и с неконъюгированным пептидом в растворе. Исследование острой токсичности препарата iRGD-MS2-Tl+ на крысах WKY (Wistar-Kyoto) показало, что однократное введение препарата iRGD-MS2-Tl+ в дозе 108 БОЕ/животное, т.е. 1.6–2.0 мкг Tl/кг, не привело к гибели ни одного животного за 3 недели наблюдения. Не выявлено заметных изменений в поведении животных. Суммарная доза Tl+, обеспечивающая достижение терапевтического эффекта (4 мкг/кг), была меньше его LD50 (20 мг/кг) в 5000 раз.
ЗАКЛЮЧЕНИЕ Направленная доставка токсичного иона металла с помощью фагового дисплея на основе частиц iRGDMS2-Tl+ в сосудистую сеть опухолевой ткани вызывает эффективный распад всей массы опухоли при значительном снижении вероятности токсического воздействия на организм в целом. Это позволяет рекомендовать iRGD-MS2-Tl+ к доклиническим исследованиям с целью создания лечебного препарата для терапии рака молочной железы. Поскольку пептидный лиганд iRGD взаимодействует с интегринами aν b3 и aν b5 на поверхности эндотелиоцитов патологической сосудистой сети [8], этот препарат может быть эффективен и в отношении других солидных опухолей, в которых идет интенсивный патологический неоангиогенез. Работа частично поддержана финансированием от ООО «Биотехнология». Разработка методик синтеза пептида (Gly)3 -iRGD и его конъюгации с бактериофагом MS2 выполнена в рамках Программы фундаментальных научных исследований государственных академий наук на 2013–2020 годы. Синтез пептида выполнен на оборудовании ЦКП «Протеом человека» (ИБМХ). Эксперименты на животных проводили в НМИЦ онкологии имени Н.Н. Петрова Минздрава РФ. Авторы благодарят А.А. Чистова (ИБМХ, ИБХ) за проведение анализа iRGD-пептида. Материалы статьи отражены в Патенте РФ № 2599462 «Способ полисигнальной активации апоптоза клеток злокачественных солидных опухолей», заявках в Патентное ведомство США (№ 15/757,285 от 02.03.2018) и Европейское патентное ведомство (РСТ – WO 2017052419).
P.S. Материал опубликован и взят с согласия ресурса http://actanaturae.ru , так как содержание данного реферата является собственностью авторов, чьё запатентованное открытие, зарегистрировано в Государственном реестре изобретений Российской Федерации от 15 сентября 2015г
Популярные Статьи
Как приготовление пищи влияет на развитие онкологии?
В настоящее время люди готовят еду разными способами. Применение газа, один из наиболее распространённых способов приготовления. Многие люди, живущие в сконцентрированном обществе, порой вынуждены гот..
Повороты судьбы и онкологические заболевания
Онкологические заболевания мира сегодня занимают вторую строчку смертности, после сердечно — сосудистых. Интересный факт, что ни сосудисто — сердечные, ни онкологичес..
Онкология лечится СТОпроцентно - Принцип работы
Статья опишет в общих чертах механизм, происходящий в лечение препаратом. В каждом организме млекопитающих присутствует группа клеток отвечающая за защиту организма от инфекции. Группа клеток называет..
Препараты для лечения рака
На сегодняшний день каждый из нас четко знает: единого и стопроцентно эффективного лекарства от рака пока не существует. Однако мнение о том, что все средства для химиотерапии и поддержания организма ..




