Ремиссия у пациента со злокачественной Мезотелиомой плевры: отчет

Абстрактный
Здесь мы сообщаем о пациенте с IV стадией злокачественной мезотелиомы плевры (МПМ), который достиг ремиссии через 5 месяцев лечения экспериментальным целевым продуктом (WO/2017/052419). Ремиссия подтверждена ПЭТ-исследованием, проведенным в немецкой клинике - как отсутствие опухолевой ткани в первичной локализации, так и отсутствие отдаленных метастазов. Лечение предыдущего пациента не было успешным. Предыдущие методы лечения включали 6 курсов комбинированной химиотерапии, состоящей из цисплатина, пеметрекседа и бевацизумаба; висцеральная и париетальная плеврэктомия в сочетании с гипертермической интраторакальной химиотерапией (хиток); 6 курсов комбинированной терапии моноклональными антителами ниволумабом и ипилимумабом. Все это лечение не продемонстрировало необходимого клинического эффекта. Терапия моноклональными антителами вызывала также тяжелые побочные эффекты-полиартрит. В связи со всеми этими причинами и значительным ухудшением общего состояния пациента и лабораторных показателей, пациент по собственному желанию начал лечение экспериментальным целевым продуктом (WO/2017/052419) в качестве единого противоопухолевого средства и через 5 месяцев достиг ремиссии. Общее состояние значительно улучшилось. Оценка ЭКоГ изменилась с 2-3 баллов в начале терапии до 0-1 баллов через 5 месяцев лечения. Пациент выполняет свои обычные обязанности в офисе.
Введение
Мезотелиома плевры-опухоль, характеризующаяся диффузным инфильтративным ростом. Диагностика мезотелиомы плевры сложна. Ее клинические проявления не специфичны, зависят от распространенности опухолевого процесса и локализации поражения. Прогноз при мезотелиоме плевры неблагоприятный, медиана выживаемости больных составляет ~12 месяцев [1] даже при агрессивном вмешательстве. Эффективность современных схем комбинированной химиотерапии (цисплатин и пеметрексед) для мезотелиомы плевры составляет 35-41% [2,3]. Такой тип опухоли демонстрирует так называемую биологическую устойчивость к химиотерапии. Именно поэтому даже просто стабилизация прогрессирования заболевания считается значительным успехом. Использование моноклональных антител для лечения мезотелиомы плевры является относительно новым подходом, и следует также рассмотреть вопросы безопасности такого лечения [4]. Таким образом, такие пациенты по-прежнему нуждаются в новых эффективных и безопасных методах лечения.
Презентация
Здесь мы сообщаем о клиническом случае пациента с эпителиоидной злокачественной мезотелиомой плевры с левой стороны. Пациент-53-летний мужчина, Белый. Диагноз был установлен в феврале 2017 года. Симптомы (температура, кашель, слабость, боль в груди) заболевания появились в конце 2016 года. Потребовалось некоторое время, чтобы провести дифференциальную диагностику с туберкулезом. Была проведена оценка возможного воздействия асбеста. Пациент выкуривал 3-6 сигарет в день.
Гистология
Опухолевая ткань имеет щелевидную форму или форму банды. Опухолевые клетки показывают относительно небольшие ядра и ядрышки, цитоплазма эозинофильна. Опухолевая ткань проникает в скелетную мышцу. Диагноз: эпителиоидная злокачественная мезотелиома плевры.
Иммуногистохимия
Опухолевые клетки экспрессируют WT1, D2-40, калретинин и CK5/6. Отсутствие выражения CEA и BerEP4. Химиотерапии начался в апреле 2017 года. Пациент получил шесть циклов комбинированной химиотерапии, состоящей из цисплатина, пеметрекседа и бевацизумаба в онкологическом отделении Медицинского центра Sheba, Израиль.
К сожалению, это лечение оказалось неэффективным. В связи с прогрессированием заболевания и ухудшением общего состояния в декабре 2017 года была выполнена левая торакотомия с резекцией перикарда, диафрагмальной резекцией, висцеральной и париетальной плеврэктомией в сочетании с гипертермией интраторакальной химиотерапией (ГИТОК).
Хирургическое вмешательство было проведено в центре пульмонологии и торакальной хирургии академическая клиника Университета Людвига Максимилиана в Мюнхене, Германия. Рецидив заболевания был обнаружен специалистами Мюнхенского центра во время экзамена на 26APR2017. Заключение и описание ПЭТ датированы 26APR2018 (Рисунок 1).
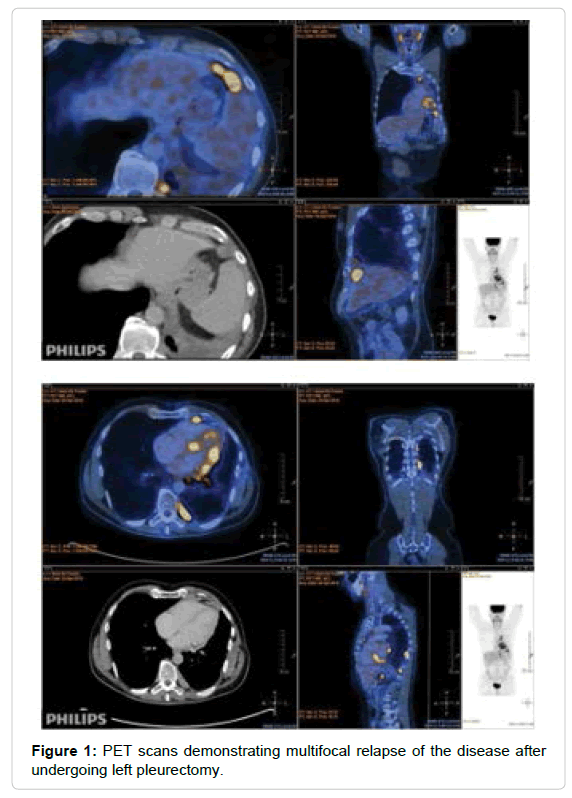
Заключение ПЭТ / КТ
ПЭТ / КТ признаки патологического метаболически активного процесса с поражением плевры слева (мезотелиома). Гиперметаболические изменения в забрюшинных и паравертебральных лимфатических узлах, чаще метастатические.
Описание:
Грудная полость: при исследовании метаболизма глюкозы соответственно определяются очаги патологической гиперфиксации радиофармацевтического препарата:
* гиперваскулярные образования в плевре, размером от 6 до 26 × 13 мм, в паравертебральных областях слева, на уровне 6-11 грудных позвонков, интенсивность накопления радиофармацевтических препаратов (SUVmax) достигает 13,13.
• "гиперваскулярными" мягкотканной процесса на плевру слева в средостении регионов, на сердца плевры (размеры до 37 × 11 мм, SUVmax до 11,24), в области переднего реберного диафрагмального синуса (до 20 × 16 мм, SUVmax до 13,69), на междолевой плевры (до 13 мм).
* гиперваскулярные образования различного размера в области среднего этажа переднего средостения, с максимальным размером 16 × 11 мм, SUVmax до 11,6. Состояние после левой плеврэктомии, средостение смещено влево, послеоперационные зажимы определяются в надфренических областях слева.
В легких без инфильтративных изменений. В базальных отделах левого легкого определяются фиброзные канатики и спайки, а в S5 слева имеется единичный очаг фиброза размером до 5 мм, без признаков гиперметаболизма глюкозы. Просвет трахеи и крупных бронхов прослеживаются. Лимфоузлы (грудные и внутригрудные) не увеличиваются, определяются одиночные переднезадние и паратрахеальные лимфоузлы до 6 мм, без признаков гиперметаболизма глюкозы. Экссудат в плевральной полости не обнаружено. Сердце и сосудистые структуры средостения Не изменены. Перикардиальный выпот не обнаружен.
Брюшной полости и малого таза: в исследовании метаболизма глюкозы в органах и тканях брюшной полости, забрюшинного пространства и малого таза, очаги повышенной фиксации РФП определяются:
* Соответственно несколько парааортальных лимфоузлов, расположенных на уровне левого надпочечника, размером от 7 мм до 13 × 11 мм, интенсивность накопления радиофармацевтических препаратов SUVmax до 10,07.
* Соответственно, одиночные паравертебральные и одиночные межпозвонковые лимфоузлы, размеры до 10 мм. SUVmax до 8.77.
Пациенту назначена комбинированная терапия моноклональными антителами:
• Ниволумаб 3 мг/кг.
• Ипилимумаб 1 мг/кг.
Пациент получил 6 циклов иммунотерапии в Мюнхенской клинике. В период апрель-июнь динамика изменений КТ была отрицательной-увеличилось количество метастазов и их размеры. За период июнь-июль-существенных изменений на КТ-снимках не произошло. Однако у больного развился тяжелый полиартрит. Это было очень болезненно и вызвало инвалидизацию пациента. Поражались большие и малые суставы. Пациент много страдал. Врачи оценили иммунотерапию как причину этого полиартрита. В начале июля пациентка прекратила иммунотерапию. В конце июля пациент в соответствии со своим добровольным решением (подтвержденным юридическим в письменной форме) начал терапию целевым продуктом (WO/2017/052419).
Через шесть недель лечения существенные позитивные изменения на КТ были обнаружены (рис. 2 и 3). Общее состояние было стабильным. Жидкость в плевральной полости, исчезли.
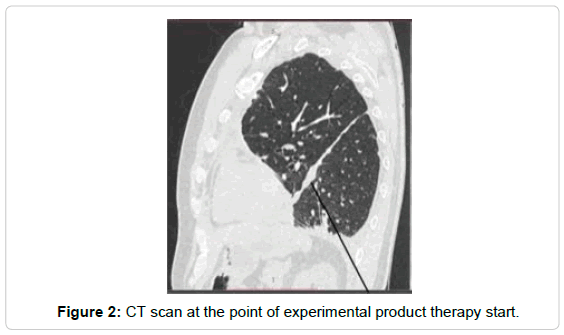
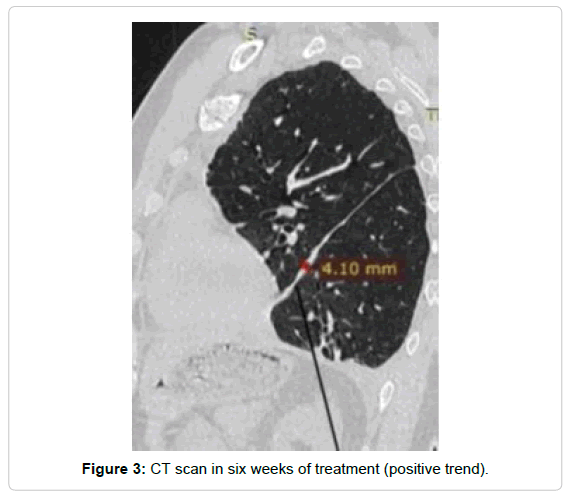
Сравнительное заключение (Рис. 3 vs Рис. 2): кт-признаки одиночного метастазирования в S5,6 левого легкого стабильны. Уменьшение размеров и количества бывших множественных метастазов в межлобарной плевре левого гемиторакса, во всех отделах грудной стенки левого гемиторакса. Уменьшение размера и количества до нормальных значений. Лимфатические узлы средостения; паравертебральные лимфатические узлы на уровне тел позвонков Th12 и L1; парааортальные лимфатические узлы на уровне брюшного отдела. По сравнению с предыдущими данными из - положительная тенденция (рис. 2 и 3).
Пациент продолжал лечение еще три с половиной месяца. Через 5 месяцев после начала терапии пациент достиг ремиссии, подтвержденной ПЭТ-исследованием, проведенным в Германии в 05DEC2018. Ремиссия подтверждена ПЭТ-исследованием на отсутствие опухолевой ткани в первичной локализации и отсутствие отдаленных метастазов.
Оценка ЭКоГ изменилась с 2-3 баллов в настоящее время начала терапии до 0-1 баллов через 5 месяцев лечения. Результат ЭГ на “5-точечный месяцев” был определен полиартрит, как побочный эффект при лечении моноклональными антителами (рис. 4 и 5). Состояние полиартрита значительно улучшилось, однако он все еще был представлен. Воспаление крупных суставов разрешилось к концу ноября. Зарегистрированные побочные явления во время экспериментального лечения оценивались как не тяжелые. Выявленные аномалии управлялись сопутствующими препаратами, вводимыми per os. Мягкая инфузионная терапия применялась в течение трех дней в течение первого месяца лечения.
В качестве справки ниже прилагается копия заключения ПЭТ, подготовленного специалистом из мюнхенской клиники. Прилагается также его перевод на английский язык. Только имя пациента и дата рождения пациента удаляются из фотографий, чтобы обеспечить конфиденциальность пациента. Для сравнения были использованы следующие результаты ПЭТ: результаты ПЭТ от 26APR2018 и 05DEC2018.

Отсутствие доказательств метаболической активности (отсутствие хранения ФДГ) в левой плевральной мезотелиоме (как в первичной опухоли, так и в предыдущих метастазах внутрибрюшного лимфатического узла или в других местах). Таким образом, можно предположить полную ремиссию. Пациент выполняет свои обычные обязанности в офисе.
Обсуждение и заключение
Сохраняется существенная потребность в альтернативных подходах к терапии MPM, поскольку результаты традиционных схем химиотерапии остаются разочаровывающими, с высокой частотой отказов и значительными профилями побочных эффектов. Здесь мы сообщаем о случае пациента с MPM, который испытал быстрое прогрессирование заболевания после стандартной химиотерапии, но имел исключительный и непрерывный ответ на терапию одним агентом WO/2017/052419. Основываясь на ответе, достигнутом у пациента, WO/2017/052419 может иметь значительные перспективы для будущей терапии MPM.
Ссылки на литературу
Marshall AD, Bayes HK, Bardgett J (2015) выживание от злокачественной мезотелиомы: где мы сейчас?. J R Coll Physicians Ed-inb 45: 123-126.
Vogelzang NJ, Rusthoven JJ, Symanowski J (2003) Фаза III исследование пеметрексед в сочетании с цисплатином против цисплатина в одиночку у пациентов со злокачественной мезотелиомой плевры. J Clin Oncol 21: 2636-2344.
Jones RG, Karthik F,Dugar A, Kanagarajan K, Desai K и др. (2018) Ниволумаб иммунотерапия при злокачественных мезотелиом: клинический случай выделяя новую возможность для исключительных результатов. Am J Case Rep 19: 783.
Марк е, Повель П, Ван-Meerbeeck Япо (2015) выявления иммунных контрольно-пропускных пунктов: новые возможности для лечения мезотелиомы?. Лечение Рака Rev 41: 914-924.
Все материалы любезно предоставлены авторами проекта и американским международным журналом
Популярные Статьи
Как приготовление пищи влияет на развитие онкологии?
В настоящее время люди готовят еду разными способами. Применение газа, один из наиболее распространённых способов приготовления. Многие люди, живущие в сконцентрированном обществе, порой вынуждены гот..
Повороты судьбы и онкологические заболевания
Онкологические заболевания мира сегодня занимают вторую строчку смертности, после сердечно — сосудистых. Интересный факт, что ни сосудисто — сердечные, ни онкологичес..
Препараты для лечения рака
На сегодняшний день каждый из нас четко знает: единого и стопроцентно эффективного лекарства от рака пока не существует. Однако мнение о том, что все средства для химиотерапии и поддержания организма ..
Онкология лечится СТОпроцентно - Принцип работы
Статья опишет в общих чертах механизм, происходящий в лечение препаратом. В каждом организме млекопитающих присутствует группа клеток отвечающая за защиту организма от инфекции. Группа клеток называет..




